94岁女性,在患有持续性房颤的基础上遭遇急性冠脉综合征,需同时使用抗凝及抗血小板药物,但其肾脏情况让医生在制订治疗方案时顾虑重重,如何做到既有效抗栓又避免出血?发生急性冠脉综合征后心功能受损,并出现肺动脉高压,这种情况下加用肺动脉高压的特异性治疗药物是否有益?每一个决策都需要仔细斟酌……
【病史摘要】
患者女性,94岁,主因“间断胸闷、心悸29年,加重4小时”,以“不稳定型心绞痛”收入院。患者于1998年起劳累后出现间断胸闷、气促,伴心悸,无心前区疼痛及放射痛。2017年3月4日午餐后出现心前区闷痛,休息后疼痛不能缓解,家人给予硝酸甘油1片含服,测血压130/60mmHg,心电图示V4~V6导联ST段压低。
既往史:高血压病史39年,血压最高为180/90mmHg,长期口服降压药,目前口服非洛地平缓释片,血压控制在130~150/70~80mmHg。2型糖尿病病史7年,口服降糖药物,血糖控制可。肾功能不全病史7年,目前诊断为慢性肾脏病3b期、肾性贫血。阵发性房扑、持续性房颤病史30年,2010年因“病态窦房结综合征、慢快综合征”行永久性起搏器植入术。
【入院时查体】
体温36℃,呼吸18次/min,脉搏68次/min,血压140/60mmHg。
颈静脉无怒张,双肺呼吸音清,无干、湿啰音。心界无扩大,心率72次/min,心律绝对不齐,第一心音强弱不等,各瓣膜听诊区未闻及病理性杂音。腹软,无压痛及反跳痛,肝肋下一指可及,脾肋下未及,肠鸣音正常。双下肢轻度凹陷性水肿,双足背动脉搏动稍减弱。
【辅助检查】
1.心肌酶
肌红蛋白定量77ng/ml,肌酸激酶35U/L,肌酸激酶同工酶7.4U/L,肌钙蛋白 I 0.030μg/L,肌钙蛋白T 0.038ng/ml,NT-proBNP 8842.8pg/ml。
2.血生化
尿素6.2mmol/L,肌酐113μmol/L,血糖7.42mmol/L,钾4.86mmol/L,钠133mmol/L。
3.血常规
白细胞计数7.16×109/L,中性粒细胞0.677,淋巴细胞0.184,血红蛋白99g/L,血小板计数246×109/L。
4.心电图
V4~V6导联ST段压低,aVR导联ST段抬高(图1)。
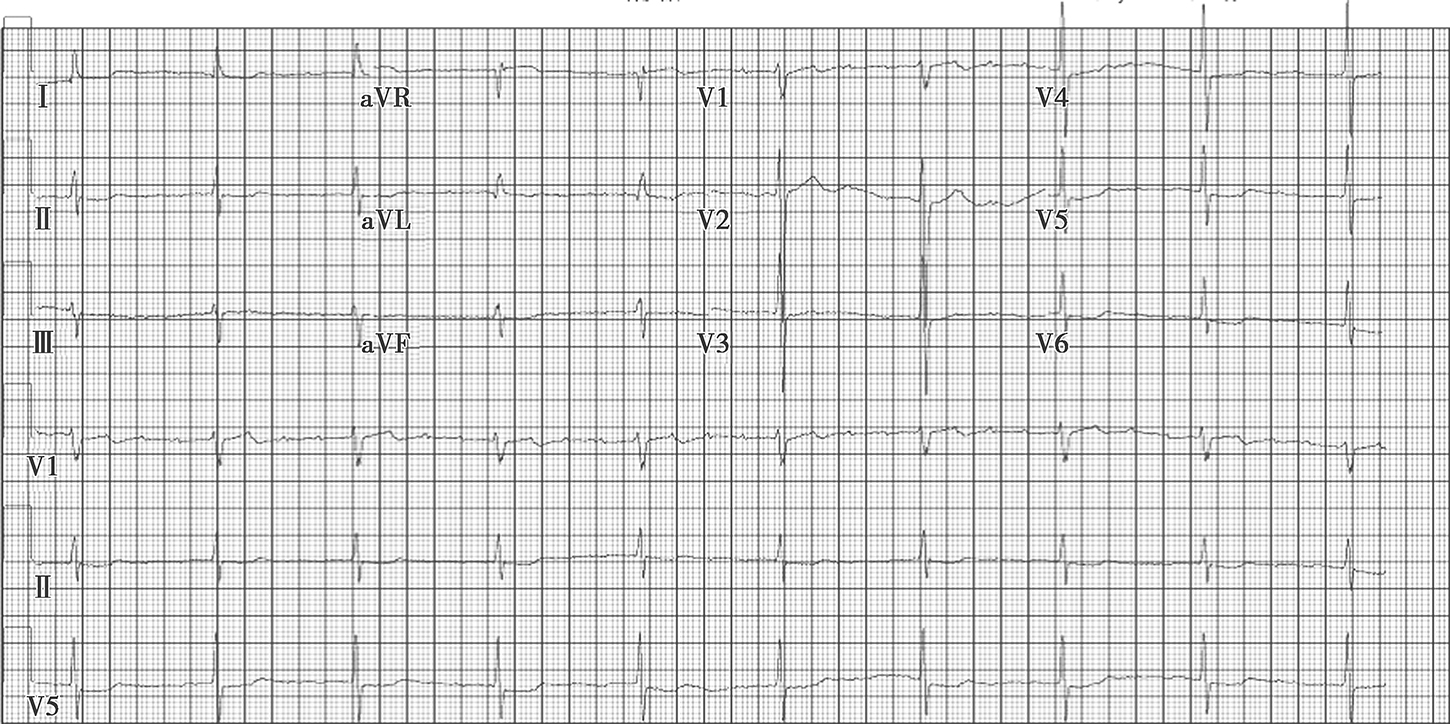
图1入院时心电图
5.超声心动图
左房内径41mm,左室舒张末内径50mm,射血分数57%。静息状态下可见左室下后壁、左室侧壁室壁回声增强、略变薄、运动轻度减弱,节段性室壁运动障碍(左室下后壁、左室侧壁)。左室整体收缩功能正常,左室整体舒张功能受损。左房轻度扩大,心包极少量积液。估测肺动脉收缩压为32mmHg。
【入院诊断】
1.冠心病,不稳定型心绞痛。
2.心律失常,病态窦房结综合征、持续性房颤、心脏永久起搏器植入术后。
3.慢性肾脏病3b期、肾性贫血。
【诊治思路及首要问题】
患者系高龄女性,心电图与超声心动图提示的心肌缺血部位吻合,动态观察心肌标志物未见升高,不除外近期发生急性冠脉综合征但心肌标志物错过检测时间窗的可能,需按照急性冠脉综合征进行治疗。但患者有持续性房颤及慢性肾脏病病史,需仔细评估其抗凝及出血风险后决定其抗栓治疗方案,以确保有效抗栓的同时防止出血并发症的发生。患者同时合并心功能不全,脑钠肽前体水平明显升高,如何加强心功能的保护,避免慢性心功能不全急性加重,也是治疗中需重点关注的地方。
【诊治经过】
根据HAS-BLED评分及CRUSADE评分,患者属于出血很高危,结合相关指南,并在密切监测下调整抗凝及抗血小板治疗方案。患者心电图与超声心动图提示的心肌缺血部位吻合,动态观察心肌标志物未见升高,不除外近期发生急性冠脉综合征(acute coronary syndrome,ACS)但心肌标志物错过检测时间窗的可能,故入院后按照ACS进行双联抗血小板及抗凝治疗,CHA2DS2-VASc评分为7分,给予阿司匹林100mg+氯吡格雷75mg+达肝素钠注射液2500U,每日1次。但患者肾功能差,既往双联抗血小板治疗时出现皮下瘀斑,HAS-BLED评分为5分,CRUSADE评分为73分,属于出血的高危患者,故阿司匹林使用2天后予以停用,保留氯吡格雷75mg+达肝素钠注射液2500U,每日1次,密切监测下未见出血发生,10天后将达肝素钠注射液加量至2500U,每12小时1次。阿司匹林停用2周后恢复使用双抗(阿司匹林100mg +氯吡格雷75mg,每日1次),停用达肝素钠,病程达1个月后停用氯吡格雷,给予阿司匹林100mg+利伐沙班2.5mg,每日1次,持续使用1年,1年后停用阿司匹林,单用利伐沙班。
入院后同时给予抗心肌缺血、营养心肌、调脂、降压、利尿等综合治疗,先后给予重组人脑钠肽及左西孟旦改善心功能,患者未再出现胸闷、胸痛发作,监测脑钠肽前体逐渐下降,1个月后(4月3日)脑钠肽前体下降至1675.2pg/ml。入院10天后(3月15日)复查超声心动图提示:左房内径46mm,左室舒张末内径52mm,射血分数56%。静息状态下可见左室下后壁、左室侧壁室壁变薄、回声增强有瘢痕形成、运动轻度减弱,符合陈旧性心肌梗死后改变,节段性室壁运动障碍(左室下后壁、左室侧壁)。左室整体收缩功能正常,左室整体舒张功能受损。左房扩大、左室略大,心包极少量积液。肺动脉高压(估测肺动脉收缩压为61mmHg)。加用贝前列腺素40μg口服,每日3次,降低肺动脉压,但患者因头痛无法耐受,使用2天后即予停用。经上述治疗后患者未再出现胸闷、胸痛发作,无心功能不全加重表现。
【最后诊断】
1.冠心病,不稳定型心绞痛。
2.心律失常,病态窦房结综合征、持续性房颤、心脏永久起搏器植入术后。
3.慢性肾脏病3b期、肾性贫血。
【随访】
复查心电图示ST段压低较前改善,基本恢复至基线水平,2018年1月24日复查超声心动图未见肺动脉高压征象。心脏情况稳定,近1年的时间未再住院。
【诊治心得】
该病例为高龄、多病共存的复杂案例。房颤患者在发生急性冠脉综合征时应如何选择抗栓治疗方案?同时合并肾功能不全时如何确定抗凝剂量?急性冠脉综合征合并射血分数保留型心力衰竭、肺动脉高压时又该如何应对?面对纷繁复杂的临床矛盾,厘清思路,综合考量,才能为患者制订合理的个体化治疗方案。
房颤是临床最常见的心律失常,其患病率随着年龄增高而增加。据估计到2050年,中国房颤患者数量将达到830万人。血栓栓塞性并发症是房颤致死、致残的主要原因。因此,抗凝治疗是房颤最重要的治疗措施。
目前建议瓣膜性房颤患者推荐应用华法林抗凝治疗,而非瓣膜性房颤患者要进行危险分层决定抗凝策略的选择。2014年ACC/AHA房颤指南推荐CHA2DS2-VASc评分系统对患者进行危险分层,其评分方案为:C,充血性心力衰竭(1分);H,高血压(1分);A2,年龄≥75岁(2分);D,糖尿病(1分);S2,卒中或TIA或体循环栓塞病史(2分);V,血管疾病(1分);A,年龄65~74岁(1分);Sc,女性(1分)。满分共9分。按照CHA2DS2-VASc方案,0分者可应用阿司匹林75~325mg/d或不抗凝,但更倾向于前者;1分者需要口服抗凝药物(新型口服抗凝药或华法林)或阿司匹林,但更倾向于前者;>2分者需使用新型口服抗凝药物或华法林抗凝治疗。然而,应用抗栓药物,最大的问题就是出血。因此,需要进行出血评分,权衡栓塞与出血的风险。
HAS-BLED出血评分是常用的预测患者出血风险的方法,其方案为:H,高血压(1分);A,肾功能和肝功能异常(各1分);S,卒中(1分);B,出血(1分);L,不稳定的INR(1分);E,老年人(年龄>65岁,1分);D,药物(合用阿司匹林、NSAID)或酒精(1或2分)。总分>3分,提示出血高危。临床上很多老年患者常常同时患有多种疾病,需要抗凝的同时出血风险也很大,导致房颤抗凝治疗遇到了尴尬局面,怎么办?ESC指南明确指出高出血风险的患者应密切关注出血情况,但不能妨碍患者接受抗凝治疗;但当HAS-BLED出血评分>3分时,应小心应用抗凝药物,并注意定期复查。
急性冠脉综合征的病理基础为动脉粥样硬化性斑块破裂或糜烂以及其继发的血栓形成。在这一过程中,血小板活化是发病的关键环节。因此,无论是在斑块破裂的急性过程,还是在防止动脉粥样硬化血栓形成的慢性过程,均需要抗血小板治疗。当房颤患者遭遇急性冠脉综合征时,需同时使用抗凝及抗血小板药物,其抗栓治疗更是让人顾虑重重。
《2017ESC急性ST段抬高型心肌梗死管理指南》中指出,房颤患者发生急性心肌梗死后,需要三联抗栓治疗方案(口服抗凝药、阿司匹林及氯吡格雷)维持使用6个月,随后继续使用二联抗栓治疗方案(口服抗凝药及阿司匹林或氯吡格雷)6个月,1年之后可考虑仅使用口服抗凝药。
新近颁发的《2018CHEST房颤抗栓治疗指南及专家组报告》中指出,对于发生ACS且同时需要口服抗凝药物的房颤患者:①若出血风险相对于复发性ACS和/或支架内血栓形成风险较低(HAS-BLED为0~2分),建议给予6个月的三联治疗,然后使用一种口服抗凝药(OAC)+一种抗血小板药物(优选氯吡格雷)的双联治疗直至12个月,之后给予OAC单药治疗;②若出血风险高(HAS-BLED≥3分),建议给予三联治疗1~3个月,然后OAC+一种抗血小板药物(优选氯吡格雷)的双联治疗至12个月,之后给予OAC单药治疗;③若出血风险极高(HASBLED≥3分、近期急性出血事件)而血栓形成风险低,建议给予OAC+一种抗血小板药物(优选氯吡格雷)治疗6~9个月,然后使用OAC单药治疗。
进一步具体谈谈药物的选择。抗凝药物可选华法林或新型口服抗凝药物(NOAC)。若使用华法林,建议INR范围在2.0~3.0,且INR在治疗范围内的时间(time in therapeutic range,TTR)>70%。NOAC目前临床试验证据支持达比加群150mg、每日2次或110mg、每日2次,以及利伐沙班15mg、每日1次。同时使用抗凝药物时,建议的阿司匹林剂量为75~100mg、每日1次,同时需使用PPI以减少胃肠道出血;P2Y12抑制剂建议使用氯吡格雷,若出血风险低,可考虑使用替格瑞洛等新型药物。
此外,还需特别关注患者的肾功能情况。据统计,在ACS患者中,30%~40%合并肾功能不全[eGFR<30ml/(min·1.73m2)]。这些患者预后不佳,住院期间出现并发症的风险增加。需要根据患者的肾功能,选择抗栓药物的类型和剂量以及造影剂用量(表1)。合并肾功能不全的ACS患者,若服用抗栓药物过量,会使得出血风险明显增加。进行直接PCI期间以及术后确保患者适量饮水,限制造影剂用量,可以很大程度上降低发生造影剂相关性肾病的风险。
表1慢性肾脏病患者急诊使用抗栓药物的推荐剂量
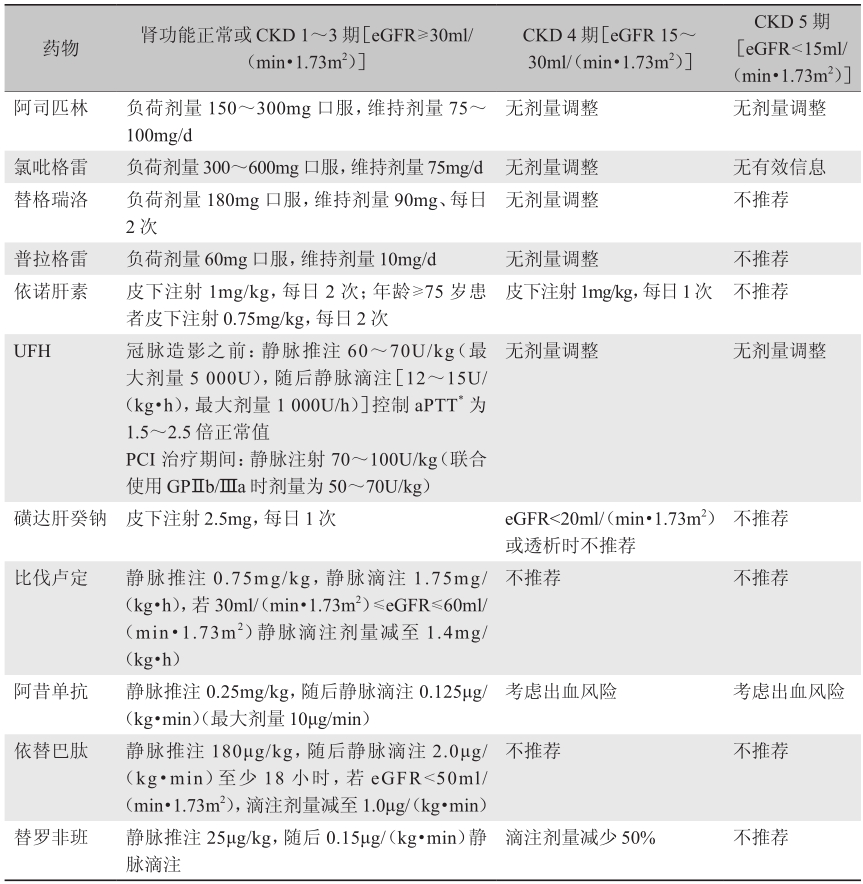
*aPTT:activated partial thromboplastine time。
对于房颤合并慢性肾脏病的患者,抗凝治疗需根据肾功能的情况进行调整。轻度慢性肾脏病(CKD 2期),CrCl 60~89ml/min,抗凝治疗与无CKD的患者相同。中度CKD(3期),CrCl 30~59ml/min,CHA2DS2-VASC≥2分的患者进行口服抗凝治疗,可选用NOAC或华法林。未接受透析治疗的重度CKD(4期),CrCl15~30ml/min,可选择华法林或NOAC,后者包括利伐沙班15mg、每日1次,阿哌沙班2.5mg、每日2次,依度沙班30mg、每日1次,基于药代动力学数据慎用达比加群。终末期肾病,CrCl<15ml/min或依赖透析,建议进行个体化选择,可选择华法林(TTR控制在65%~70%),一般不应使用NOAC(表2)。
表2慢性肾脏病合并房颤患者的抗凝选择
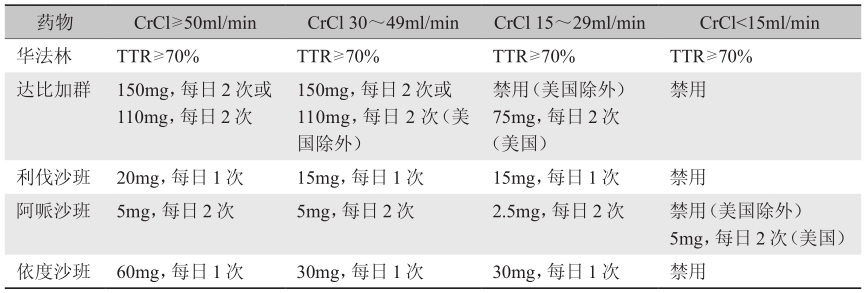
该病例为高龄女性患者,CHA2DS2-VASc评分为7分,房颤卒中发生的风险极高,必须给予抗凝治疗,但患者同时合并慢性肾脏病3b期,HAS-BLED评分为5分,出血风险也极高,在此基础上发生了ACS,需同时进行抗血小板治疗,联用抗血小板及抗凝药物会使得出血风险进一步升高。因此,其抗栓治疗必须从小剂量开始,严密监测下采用个体化方案。按照本病例的治疗方案,采用药物小剂量联合抗栓治疗,加用PPI预防出血,患者ACS治疗效果满意,未发生明显临床出血征象。
随着人口老龄化,老年心力衰竭患者发病率增长。在65岁以上的慢性心力衰竭患者中,超过50%的患者为射血分数保留的心力衰竭(HFpEF);在老年女性患者中,约80%的新发心力衰竭为HFpEF。《2016ESC急慢性心力衰竭诊疗指南》将心力衰竭分为3种类型:射血分数减低型心衰(HFrEF,LVEF<40%)、射血分数中间值的心力衰竭(HFmrEF,LVEF 40%~49%)和射血分数保留型心衰(HFpEF,LVEF≥50%)。HFpEF的诊断需满足以下条件:存在心力衰竭的症状和体征;左心室收缩功能正常,LVEF≥50%;BNP水平>35ng/L和/或NT-proBNP水平>125ng/L;存在心脏结构及功能受损的客观依据;左心房扩大和左心室肥厚,但左心室不大,舒张功能不全。由于BNP和NT-proBNP血浆水平随着年龄增长而升高,而且老年患者常合并多种疾病,高血压等合并症也会引起左心室重构。因此,老年HFpEF的诊断面临着巨大挑战。根据指南制定的诊断标准,该患者HFpEF的诊断成立。
老年HFpEF的治疗目标为:延缓症状和体征、提高脏器功能和生活质量、预防急性加重和相关再住院、延长寿命。药物治疗方面,利尿剂能够改善老年HFpEF患者的症状,但不能改变预后。因此,《2016ESC急慢性心力衰竭诊疗指南》推荐使用利尿剂来缓解HFpEF患者的症状和体征(Ⅰ类推荐,B级证据)。尚无证据提示RAAS系统拮抗剂能够缓解症状、改善预后、减少全因死亡。螺内酯治疗并不能降低由心血管死亡、复苏的心脏骤停、心力衰竭住院等组成的复合终点事件发生率;但似乎可以降低再住院率,可以考虑使用。β受体阻滞剂在HFpEF患者缓解症状和改善预后方面并没有足够的证据。有研究显示,奈必洛尔在老年患者中可能减少死亡和再住院的复合终点事件。EDIFY研究结果提示,伊伐布雷定降低心率并不能改善预后;Medicare-linked OPTIMIZE-HF研究结果提示,出院时心率低与低死亡率相关,但与未来再住院率无关。西地那非不能改善HFpEF患者的生活质量。
肺动脉高压(pulmonary hypertension,PH)是临床中常见的疾病,在各种肺动脉高压的病因中,又以左心功能衰竭相关的肺动脉高压最为常见。左心疾病所致的肺动脉高压(PHLHD)占所有肺动脉高压患者的65%~80%。另一方面,左心功能衰竭患者出现肺动脉高压和右心功能不全,对疾病的进展、预后及死亡率有着重要的影响。因此,心力衰竭合并肺动脉高压应引起心血管医师的足够重视。
心力衰竭合并肺动脉高压时,左心功能障碍导致左心充盈压升高,进一步导致肺静脉压力升高、肺淤血、肺循环阻力增加,随着病程的进展和压力的传导,肺动脉发生血管内皮功能障碍,出现反应性的血管收缩,神经内分泌的激活导致肺小动脉重构、炎症细胞激活、NO减少、内皮素分泌增加、钠尿肽的舒张血管作用降低,进一步导致肺血管重构的发生,肺动脉高压形成,最终导致右心室的后负荷增加以及右心功能衰竭。
左心衰竭合并肺动脉高压的患者,可以根据患者的危险因素、基础心脏疾病、临床表现,以及由非侵入性到侵入性的辅助检查方法,逐步明确诊断。如患者有老年、高血压、2型糖尿病、冠心病、体重指数(body mass index,BMI)>30kg/m²等危险因素,或有肺水肿、端坐呼吸的临床表现;心电图改变提示左室肥厚、电轴左偏、房颤;超声心动图提示左房扩大、左室肥厚、左室收缩/舒张功能不全征象、瓣膜病;胸部X线检查提示肺充血、KerleyB线、胸腔积液、左心扩大;心肺运动试验中呼气末二氧化碳(PETCO2)在无氧阈中正常或轻度降低,运动时不降低,VE/VCO2在运动时不增加;以上均支持心力衰竭合并PH。该患者为高龄老年,既往无肺动脉高压病史,HFpEF诊断明确,在ACS发生后的病程中,超声心动图监测肺动脉压明显升高,出现HFpEF合并PH。
心力衰竭合并肺动脉高压的治疗主要包括两个方面。
1.针对左心衰竭的治疗
肺动脉高压的治疗仍以治疗左心功能衰竭、降低左心充盈压为主。心血管疾病及代谢综合征的危险因素控制;针对左心衰竭予以优化的药物治疗方案(血管紧张素转化酶抑制剂、β受体阻滞剂、醛固酮抑制剂等),达到目标剂量;减轻容量负荷的治疗(利尿剂);器械治疗(CRT、ICD、冠心病的血运重建、左室辅助装置);导致PH的其他合并症的识别和治疗,如慢性阻塞性肺疾病、睡眠呼吸暂停和肺栓塞。CHAMPION试验表明,降低PAP可作为减少HFrEF和HFpEF患者再入院率的治疗目标,但研究中PAP的降低不通过PH的特异性药物实现,而通过心力衰竭优化药物治疗包括利尿剂的合理使用达到。
2.PH的特异性药物治疗
支持PH的特异性药物治疗心力衰竭合并肺动脉高的证据主要来自一些急性或者短期的研究,包括使用前列腺素类、内皮素受体拮抗剂及5型磷酸二酯酶抑制剂。大多数试验表明,这些药物可以改善患者的血流动力学、运动耐量以及症状。但由于这些试验存在很多局限性,包括样本量小、单中心、不完全的随机分组等,使得试验结果的可靠性不强。
目前进行的大型临床随机对照试验使用PH的特异性药物治疗心力衰竭获得的结果并不理想。FIRST试验静脉用依前列醇治疗HFrEF合并PH的患者,但由于治疗组的患者有死亡率增加的趋势,而被迫提前终止试验。MELODY试验(NCT02070991)针对存在混合性肺动脉高压(combined post and precapillary pulmonary hypertension,Cpc-PH)的HFpEF患者使用新型的内皮素受体拮抗剂马西替坦(macitentan)治疗的安全性及有效性研究,正在进行Ⅱ期临床试验。RELAX试验表明,5型磷酸二酯酶抑制剂西地那非治疗HFpEF但不合并PH的患者,不能改善其峰值氧耗及运动耐量。一个单中心的随机对照试验使用西地那非治疗HFpEF合并单纯毛细血管后肺动脉高压(isolated post-capillary pulmonary hypertension,Ipc-PH)的患者,结果表明西地那非不能够改善患者的血流动力学及运动耐量。多中心的西地那非治疗心力衰竭合并肺动脉高压的研究SilHF试验(NCT01616381)正在进行当中。
LEPHT试验使用鸟苷酸环化酶激动剂利奥西呱治疗HFrEF合并PH的患者,虽然结果表明药物可降低肺血管阻力(pulmonary vascular resistance,PVR)、提高心指数,但最终因无法达到与安慰剂相比降低PAP的主要终点而以失败告终。DILATE试验针对利奥西呱治疗HFpEF合并PH的患者也得到了类似的结果。这些结果表明,利奥西呱对系统或心脏的作用效果可能超过其舒张肺血管的作用。
从病理生理角度看,PH的特异性药物治疗可能会导致肺动脉扩张,增加肺血流,导致左心充盈压升高,潜在可能导致肺水肿和加重左心失代偿。因此,基于目前的证据,指南对心力衰竭合并肺动脉高压仍不推荐使用PH的特异性药物治疗心力衰竭。
该患者在出现肺动脉高压后,加用了贝前列腺素口服降肺动脉压治疗,但因出现头痛无法耐受,2天后即予停用。治疗方面,主要给予抗栓、抗心肌缺血及抗心力衰竭治疗。通过针对ACS及心力衰竭的一体化治疗后,患者心功能明显改善,监测脑钠肽前体从入院时的8842.8pg/ml下降至1个月后的1675.2pg/ml,而后续再复查超声心动图时未再见肺动脉高压征象。上述提示,当心力衰竭合并肺动脉高压时,纠正加重心衰的诱因并积极抗心力衰竭治疗是关键、有效的治疗措施,是否使用肺动脉高压的特异性治疗药物在其中无足轻重。
小贴士
老年人多病共存是普遍现象,诊疗过程中常常面临多重矛盾,临床医生需要仔细甄别主要矛盾,保证患者安全。
血栓与出血这对矛盾一直以来是心血管领域的热点话题,当房颤、ACS、肾功能不全同时存在时,联合抗栓方案必须做到高度个体化,加强出血监测,并采取适当的预防措施。
肺动脉高压在老年人群非常常见,以左心疾病相关的肺动脉高压为主。左心功能衰竭合并肺动脉高压和右心功能不全时往往提示预后不良,需引起足够的重视。
对于HFpEF合并肺动脉高压患者,治疗侧重原发病及心力衰竭的治疗,不推荐使用肺动脉高压靶向药物治疗。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。 此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
