76岁男性,因急性心肌梗死行急诊PCI,术后9天发现大量心包积液,原因是什么?PCI术后血压持续偏低、IABP难以撤机的原因是什么?心包积液迁延1年余,有没有其他原因?如何鉴别?
【病史摘要】
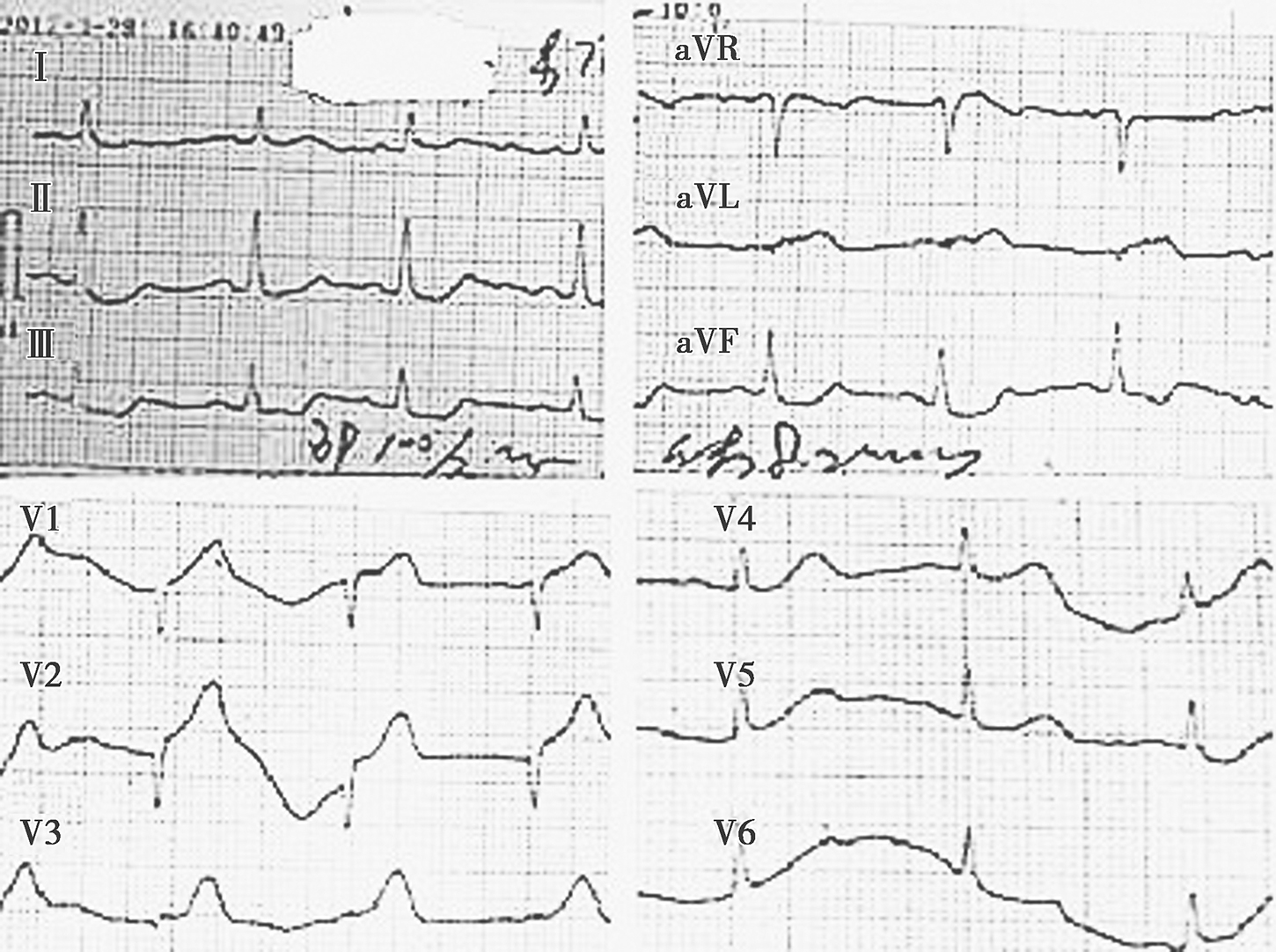
图1发病时心电图
患者男性,76岁,主因“突发胸闷、胸痛9天,发现大量心包积液1天”以“冠心病,急性前壁心肌梗死、PCI术后、心包积液原因待查?” 于2017年4月6日收住院。2017年3月28日患者在下棋过程中(16:00)突发胸痛,呈压榨样,伴胸闷、大汗,自行含服速效救心丸不能缓解,至就近医院急诊就诊,查心电图示V1~V4导联ST段抬高,V1~V3导联R波递增不良(图1),考虑为急性前壁心肌梗死。17:30入导管室行冠状动脉造影及PCI术,冠脉造影(图2)示冠脉左优势,右冠近段闭塞,前降支开口99%狭窄伴血栓影,中远段80%狭窄,TIMI血流1~2级,在IABP支持下于前降支开口植入3.0mm×15mm Resolute支架1枚,复查造影示TIMI血流3级,心包未发现造影剂渗漏。术后给予强化抗栓治疗,具体方案为替罗非班(1/3常规量)静脉泵入持续24小时;达肝素钠5000U皮下注射,每12小时一次;阿司匹林肠溶片100mg,每日1次;替格瑞洛90mg,每日2次。术后患者血压偏低,持续使用IABP,并给予多巴胺静脉滴注维持血压。治疗期间两次复查心脏超声示心功能改善(3月29日示LVEF 35%;4月1日示LVEF 44%),均未见心包积液。4月4日患者出现心率增快,波动于90~115次/min,间断胸闷,伴恶心、呕吐,给予毛花苷C(0.4mg分次静脉推注)及利尿剂治疗,症状无明显改善。4月6日(心肌梗死第9天)复查心脏超声示大量心包积液(前心包18mm,后心包7mm,侧心包19mm),患者心肌梗死面积大,考虑心脏破裂的可能,为进一步诊治于2017年4月6日转入我院。

图2急诊冠脉造影及PCI
A.右冠近段闭塞;B、C.前降支开口99%狭窄伴血栓影;D、E.前降支开口植入3.0mm×15mm Resolute支架1枚;F.心包未发现造影剂渗漏。
既往史:1977年曾诊断为肺结核。无高血压、糖尿病病史。体检发现肝巨大囊肿、胆囊结石、胆管结石。1964年行阑尾切除术。无烟、酒嗜好。
【入院时查体】
脉搏112次/min,血压波动在90~120/50~70mmHg(IABP支持)。
颈静脉充盈,双肺呼吸音清晰,未闻及明显干、湿啰音。叩诊心界向双侧扩大,心率112次/min,律齐,心音遥远,各瓣膜听诊区未闻及病理性杂音。腹部平坦,未触及压痛,肠鸣音4次/min。双下肢无水肿。
【辅助检查】
1.血常规
白细胞计数12.76×109/L,中性粒细胞0.832。
2.血生化
C反应蛋白2.35mg/dl,肌红蛋白、肌酸激酶同工酶正常范围,肌钙蛋白I 2.667μg/L,肌钙蛋白T 0.779ng/ml,NT-proBNP 2011.9pg/ml。
3.心电图
窦性心动过速,心率107次/min,V1~V4导联异常QRS,ST-T段改变。
4.超声心动图(2017年4月6日)
静息状态下可见左室前间壁心尖段、室间隔及左室前壁心尖段室壁变薄(约4mm),回声偏低,运动明显减弱;心包检查可见中-大量液性暗区包绕心脏,心脏呈“摆动征”;右房、右室受压变小(图3)。
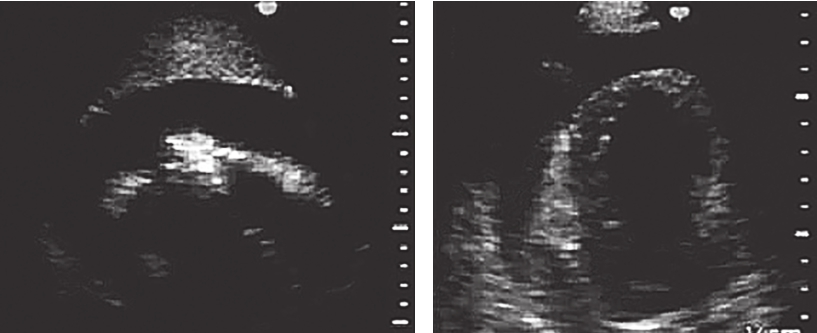
图3入院时超声心动图
【入院诊断】
1.冠心病,急性前壁心肌梗死、前降支PCI术后Killip 1级、心包积液原因待查?心脏破裂可能性大。
2.陈旧性肺结核。
3.阑尾切除术后。
4.肝囊肿。
5.胆囊结石、胆管结石。
【诊治思路及首要问题】
该病例急性ST段抬高性心肌梗死的诊断明确,梗死面积大,已接受了紧急血运重建(前降支支架植入),PCI术后9天复查心脏超声发现大量心包积液。首要解决的问题:①查找心包积液的原因:患者有介入治疗史,首先需要排除介入并发症可能,回看患者造影光盘,在PCI操作完成后复查造影未见到造影剂渗漏入心包,说明心包积液非介入并发症;②心脏破裂:患者处心肌梗死急性期,为前壁梗死,且梗死面积大,是发生机械性并发症的高危人群,应重点排查;③查找患者发病后血压持续偏低、IABP难以撤机的原因:心包积液导致心脏限制性充盈障碍,回心血量下降,是影响血压的原因之一;心肌梗死后低血压的鉴别诊断还包括心源性休克、右心室梗死、心室游离壁破裂、室间隔穿孔、低血容量等原因,结合该患者情况应如何判断;④若急性心肌梗死合并心脏破裂的诊断成立,治疗上应紧急外科手术还是内科保守治疗。
【诊治过程】
患者入心脏监护室,继续给予抗血小板、抗心肌缺血、调脂及保护心功能等综合治疗,4天后IABP成功撤机。
第一阶段(2017年4月6日至2017年6月13日):患者处心肌梗死急性期、PCI术后,正在使用双联抗血小板治疗,如行心包穿刺需停用抗血小板药,发生支架内血栓的风险较大,故未行心包穿刺。多次复查心脏超声示大量心包积液持续不吸收。患者血压波动在90~100/50~60mmHg,但无头晕、胸闷、胸痛、气促等不适。
第二阶段(2017年6月14日至2018年7月2日):为进一步诊断及治疗,于2017年6月14日行第一次心包穿刺(图4),共引流出血性心包积液560ml,复查心脏超声示心包积液消失,但3个月后病情反复,复查心脏超声再次出现大量心包积液,分别于2017年9月和2018年1月、4月、6月行四次心包穿刺,心包积液引流量分别为1370ml、590ml、920ml、970ml,均为血性积液,多次完善结核、自身免疫、肿瘤等相关检查,均无阳性发现。2018年先后2次行心肌声学造影,未见造影剂外渗。2018年6月4日进一步行心脏增强磁共振成像(图5),结果示心包腔大量积液,右心室游离缘中间部分右室腔内自心包腔至右心室方向少量湍流信号,不除外右室游离缘微小破裂孔;右室壁不均匀增厚伴强化,考虑为心包积液后粘连性心包炎改变。6月15日举行院内外联合会诊,考虑患者心包积液来源于心肌微小裂孔所致血液渗出的可能性大,有外科开胸探查指征,且患者冠脉病变未完全再血管化,拟同时行冠状动脉旁路移植术。
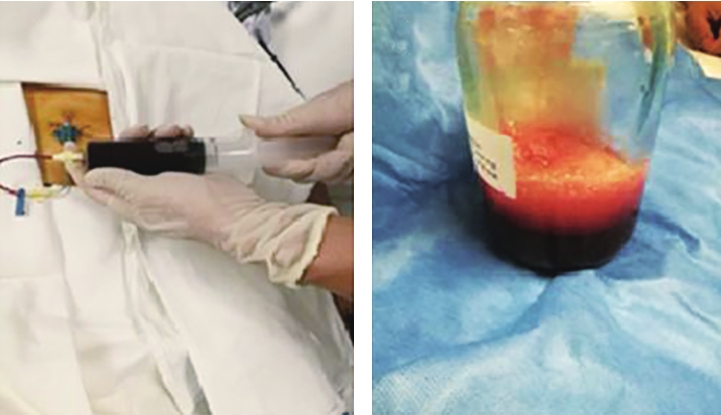
图4第一次心包穿刺所见
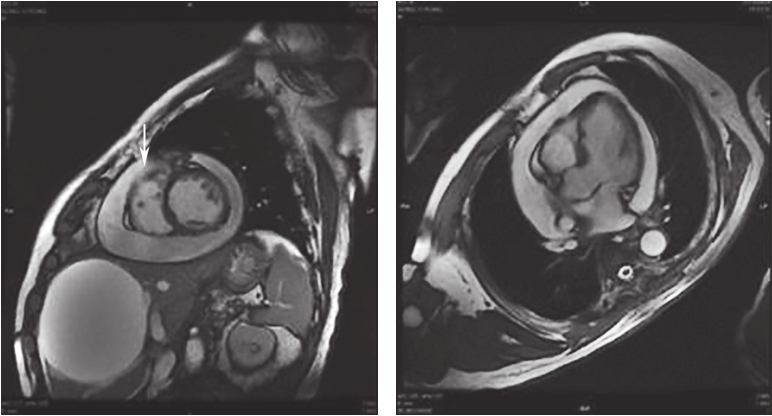
图5心脏增强磁共振成像所见
第三阶段(2018年7月3日至出院):2018年7月3日行开胸探查+冠状动脉旁路移植术,术中所见右室前壁靠近心尖处,心肌梗死与正常心肌交界处可见持续渗液,范围为3cm×1cm,予以牛心包补片连续缝合修补渗液处;切除两侧心包至膈神经前方,并打开左侧胸腔与心包腔相通;前降支支架处附近,心肌表面和心包有5cm×5cm的粘连,粘连处心包边缘进行加固缝合;右侧房室沟处2cm×2cm的心脏表面心包粘连,粘连加固缝合;乳内动脉→前降支旁路移植,肺动脉压由37mmHg减至20mmHg。术后予以阿司匹林+氯吡格雷双联抗血小板治疗,并留置胸腔引流管,引流液逐渐减少,1周后拔除引流管,康复出院。
【最后诊断】
1.冠心病,急性前壁心肌梗死、右室心肌梗死、前降支PCI术后、右心室前壁破裂心包补片缝合术后、心包及左侧胸腔开窗术后、CABG术后。
2.陈旧性肺结核。
3.阑尾切除术后。
4.肝囊肿。
5.胆囊结石、胆管结石。
【随访】
术后定期随访,未见心包及胸腔积液。
【诊治心得】
该病例在发生急性前壁心肌梗死的第9天发现心包积液,当时考虑心脏破裂的可能性大,但是早期未能找到心脏破裂的直接证据,给予心包穿刺放液对症处理,病程迁延,探寻病因的过程长达1年余,先后行5次心包穿刺,最终开胸探查证实为右室游离壁(前壁)破裂所致心包积液,病因为左室前壁心肌梗死波及右室,属临床罕见病例。
心脏破裂是急性心肌梗死(acute myocardial infarction,AMI)后的致死性并发症之一,因破裂部位不同而分为室间隔穿孔、游离壁破裂、乳头肌腱索断裂等,常导致急性心力衰竭、心脏压塞等危急情况,一旦发生,患者病死率高达75%以上,是AMI早期死亡的主要原因。心脏破裂常见于AMI发病后5天内,尤以24小时内最为多见,其次是7~14天,很少在14天以后出现。晚期心脏破裂常发生在心肌梗死后数天到数周,与多支血管病变有关。心脏破裂的发生部位常位于正常心肌和梗死心肌的交界处,以前壁与室间隔的交界处或心尖部最易发生破裂,这两个部位在心脏收缩时所承受的压力最大。
急性心肌梗死并发右室游离壁穿破少见,发生率仅为左室游离壁穿破的1/7。1952年Oblacth等总结13 665例尸检报告,其中1 026例存在心肌梗死,心脏穿破者80例,其中右室壁穿孔者仅3例,均见于大面积右室梗死和室间隔穿孔。
单纯右室梗死少见,仅占急性心肌梗死发生率的2.4%左右,最高报道为3%。右心室梗死绝大多数与左室梗死并存,包括左室下壁合并右室梗死、左室下壁合并孤立性右室乳头肌梗死、左室前壁合并右室梗死、左室侧壁合并右室梗死、左室心内膜下合并右室梗死以及左室复合梗死合并右室梗死。最常见的类型是左室下壁梗死延伸至右室后壁,有20%~45%的左室下壁梗死并存右室梗死;其次是左室前壁梗死延伸至右室前壁,可达13%。
左室前壁梗死波及右室,早在20世纪30年代经解剖发现,尸检结果显示此型右室梗死中,左室前壁心肌损失量大,对室间隔的累及更为严重。Cabin检查了连续3年的左室前壁梗死心脏标本共97例,发现其中13例合并右室前壁梗死(13%),但生前无一例拟诊为右室梗死,他们发现所有右室前壁梗死是左室前壁梗死的延伸,累及室间隔前部。通常认为,右室游离壁前壁有右冠脉圆锥支和左前降支的右室支双重供血,一般情况下不易发生梗死。Jame曾详尽研究82例右室这部分冠脉的血供情况,特别指出左前降支在这一区域供血的重要性。Cabin等研究表明,91%的心脏右室前壁部分血液供应来源于左前降支,在24%的心脏,右室前壁的30%或30%以上由左前降支供血。此型右室梗死,与左前降支高度狭窄及多发性血栓造成左前降支管腔完全闭塞明显相关。
该病例急性前壁心肌梗死的诊断明确,冠脉造影显示左优势冠脉,右冠近段闭塞,前降支开口99%狭窄伴血栓影,中远段80%狭窄。考虑本次发病的罪犯血管为前降支,予行支架植入。开胸探查可见右室前壁靠近心尖处,心肌梗死与正常心肌交界处持续渗液,范围3cm×1cm,至此确诊为右室前壁破裂所致心包积液,原因为左室前壁梗死波及右室。这一发现与患者造影结果吻合,因冠脉分布呈左优势型,左回旋支无重度狭窄,右室下壁的血液供应正常,右冠近段闭塞,右室前壁血液供应依赖于左前降支,在前降支存在重度(99%)狭窄伴血栓形成的情况下,左室前壁和右室前壁的供血同时受到影响,导致左室前壁梗死合并右室梗死。这一诊断也可以解释患者在急诊PCI术后仍持续低血压、IABP撤机困难的原因,即存在右室缺血和梗死。右冠近端阻塞是右室梗死形成的关键,因为这将危害到供应右室游离壁的右室支血管。右室功能障碍的程度与右室支血流受损的程度相关,右室支血运重建失败将导致右室功能无法恢复,持续低血压、低心排血量及高死亡率。
左室前壁右室梗死的超声心动图特征为于心尖四腔心切面显示室间隔心尖段运动异常,并延续至右室心尖部,可累及右室游离壁近心尖区。右室心尖部运动异常区呈正三角形,宽底在右室心尖1/3处,梗死顶部指向心底部。右室游离壁破裂的超声心动图表现为:①右室游离壁破口对应的心包腔内可见不同程度的液性暗区;心包腔内液性暗区迅速增宽为心脏压塞的特征性图像改变,彩色多普勒于相应切面可见心包腔内液性暗区中红或蓝色血流束,由穿孔处至心包腔;②穿孔的室壁可于相应心腔切面上呈现心室壁回声中断;穿孔部位的心肌较薄且运动失常;③由于心包腔内压力增高,心室收缩力减弱,穿孔处的血流速度多较低。心肌破裂处无论位于前壁或下壁,均为纵行裂口,表层裂口较大,里层较小,常常形成迂曲不整的孔道。由于右室解剖形态的特殊性,并受常规心脏超声切面观察角度的局限,本例患者多次超声检查均未能明确破口位置,是诊断困难的原因之一。心包积液临床症状的发生主要是由于大量心包积液压迫心脏和周围器官及组织所引起,取决于心包腔内的液体量、液体蓄积增加的速度和心包的特征。当心包腔内液体量缓慢增加时,有一定弹性的心包被扩展以接受所增加的液体量,而心包腔内压力几乎不变。在此情况下,心包腔内液体蓄积可达2000ml而不引起心包腔内压力升高。相反,若心包腔内液体量增加迅速,即使200ml也可引起心包腔内压力急剧升高,使心脏受压而产生血流动力学变化。本例患者第一次心包穿刺引流量为560ml,此后间隔2~3个月定期复查并先后行4次心包穿刺,引流量分别为1370ml、590ml、920ml、970ml,性质相同,均为血性心包积液。曾反复行肿瘤、结核及其他病原学相关检查,未见阳性发现。考虑存在超声无法探明的心肌梗死后心肌微小破裂,保守治疗未能正常愈合,致血液持续渗出心包腔,为了证实这一推论,又对患者进行了心肌声学造影及增强磁共振成像,结果示心肌声学造影无异常发现,增强磁共振成像可见存在心包腔至心室方向的湍流信号,提示心肌微小裂孔的可能。因右室压力显著低于左室,渗液速度缓慢,故未引起急性心脏压塞症状,是临床诊断的干扰因素,也是患者得以幸存的原因。
由于冠状动脉供血的区域特性,右室梗死可以是不同程度不同范围左室梗死的延伸。右胸导联心电图ST段抬高被认为是急性右室坏死的一个特异指标,在发病早期对检出左室下壁梗死并存的右室梗死有很高的敏感性和特异性。对左室前壁心肌梗死合并的右室梗死,其右胸心电图研究开始较晚。在大面积左室心肌梗死伴小面积右室梗死时,可以使大多数右胸导联的ST段压低。Adersen等认为,右胸导联ST段抬高≥1mm对急性右室梗死的诊断价值就不同类型的心肌梗死而言是不同的。还需要提及的是,ST段抬高的时间持续较短,最快甚至在胸痛发作2小时内消失。防止漏诊右室梗死的最简单方法是对下壁和/或真后壁梗死患者行常规右胸心电图检查,该检查可以检出并存右室梗死的绝大多数患者,可能遗漏的是右胸导联抬高的ST段下降极快(1.5小时)的个别患者和就诊时间晚(发病超过10小时)的患者,但此缺陷能被头胸导联右胸心电图所纠正。对于有右心衰竭或休克的急性左室前壁梗死患者,应想到合并右室梗死的可能性,此类患者可因大面积左室梗死掩盖右室梗死的存在。该病例在发病初期未及时采集右胸导联心电图,是右室梗死漏诊的可能原因之一。
临床上,左室前壁梗死合并右室梗死导致“压力泵”功能严重损害,而左室后壁梗死合并右室梗死时导致“容量泵”功能严重损害,前者引起的心源性休克的救治难度高于后者。该病例的情况属于前者,幸运的是,其在急性期接受了紧急PCI,对罪犯血管及时进行了血运重建,冠脉血液供应得以恢复,并在早期启动IABP维持血压、改善冠脉和肾脏等重要脏器灌注,是救治成功的关键措施。
心脏破裂一旦确诊,外科干预是唯一具有决定性效果的治疗方式。从手术的操作方式上来说,目前主要包括梗死灶切除+补片缝合、大补片直接缝合覆盖破损处及无缝线补片胶水粘合等。无缝线补片胶水粘合技术是应用DACRON和TEFLON补片覆盖破裂处、坏死区域及周围的正常心肌组织,这种补片不需要缝合固定,而是通过氰基丙烯酸酯胶粘合,具有可有效封堵住破裂处、保持原有的心室容积等优点,已成为治疗心脏游离壁破裂的首选治疗方法。该病例临床分型属于亚急性游离壁破裂(渗出型),心脏压塞症状相对较轻。随访1年余,患者心包积液反反复复,提示心脏破口未修复,此时完善心脏增强磁共振成像提示右室游离缘微小破裂孔。开胸探查证实了术前诊断,术中所见右室前壁靠近心尖处,心肌梗死与正常心肌交界处可见持续渗液,范围为3cm×1cm,予以牛心包补片连续缝合修补渗液处,最终患者心包积液的问题得以成功解决。
小贴士
心脏破裂是急性心肌梗死的严重并发症,死亡率高。心脏破裂的发生部位常位于正常心肌和梗死心肌的交界处,以前壁与室间隔的交界处或心尖部最多见。急性心肌梗死并发右室游离壁穿破少见。
右心室梗死绝大多数与左室梗死并存,最常见的类型是左室下壁梗死延伸至右室后壁,有20%~45%的左室下壁梗死并存右室梗死;其次是左室前壁梗死延伸至右室前壁,可达13%。
超声心电图是诊断心脏破裂的重要工具。由于右室解剖形态的特殊性,并受常规心脏超声切面观察角度的局限,本例患者多次超声检查均未能明确破口位置,是诊断困难的原因之一。
防止漏诊右室梗死的最简单方法是对下壁和/或真后壁梗死患者行常规右胸心电图检查。
心脏破裂一旦确诊,外科干预是唯一具有决定性效果的治疗方式。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。 此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
