胃肠间质瘤(gastrointestinal stromal tumors,GIST)的淋巴结转移较少,特别是在成人GIST患者中罕见。但其在儿童患者中发生率较高,且常见于SDH缺陷型患者。中国GIST诊治专家共识及NCCN指南均推荐,GIST手术不必常规行淋巴结清扫。目前GIST淋巴结转移与其预后的关系尚不十分明确,本例介绍一例c-KIT基因突变、伴淋巴结转移的胃GIST病例,以供大家参考。
【病例摘要】
患者,女性,59岁,2017年1月8日因“间断腹胀、腹痛1周余”就诊于当地医院,行腹部CT示:胃充盈欠佳,胃壁增厚。胃镜检查示:胃小弯侧巨大新生物,胃肿瘤可能。患者为求进一步诊治,于2017年4月10日至华中科技大学同济医学院附属协和医院胃肠外科就诊,患者自诉起病来不伴黑便、发热等症状,门诊以“胃占位性病变”收治入院。
既往史及家族史
既往2型糖尿病史10余年,使用药物控制良好,余无特殊。否认手术史、外伤史,否认食物、药物过敏史;父母已故;家族中无类似疾病史。
体格检查
患者皮肤黏膜苍白,未见黄疸,未触及浅表淋巴结肿大。腹部平坦,未见腹壁静脉曲张,未见胃肠型及蠕动波;腹软无抵抗,肝脾肋下未触及,未触及明显腹部包块,Murphy征(-),移动性浊音(-),肠鸣音约5次/分。双下肢轻微水肿。
辅助检查
血常规:白细胞 5.93×109/L,红细胞 3.70×1012/L↓,血红蛋白 97g/L↓,血小板 341×109/L,中性粒细胞百分比 49.00%,淋巴细胞百分比 37.60%。
血生化:总蛋白 61.3 g/L↓,白蛋白 34.8 g/L↓,ALT10U/L,AST14U/L。余指标均在正常范围内。
肿瘤标志物:未见明显异常。
全腹部增强三维CT:①胃底-胃体小弯侧胃壁不均匀增厚,多发溃疡形成,浆膜面稍模糊毛糙,肝胃韧带区见少许淋巴结,其中一枚增大淋巴结边缘模糊,长径约1.1cm;所见多考虑胃癌,影像学分期T3~4aN1Mx;②肝右后叶见边缘模糊的类圆形稍低密度影,直径约1.1cm,强化不明显;不除外转移瘤,建议MRI检查;③子宫及双侧附件区未见明显异常密度影;④腹盆腔及腹膜后未见肿大淋巴结。
肝脾增强MRI:①肝脏S6~S7段交界见直径约1.2cm的类圆形长T1长T2信号影,中央T2信号更高,DWI呈环状弥散受限,增强扫描边缘强化,考虑肝转移瘤;②增强扫描动脉期肝内散在小结节状、小片状明显强化影,余各期呈等信号,多考虑一过性灌注异常;③胃底-胃体小弯侧胃壁不均匀增厚,可见宽大溃疡,浆膜面欠光整,胃小弯侧见少许淋巴结,考虑胃癌,建议结合内镜检查结果分析;④肝门及腹膜后未见明显肿大淋巴结(图1)。
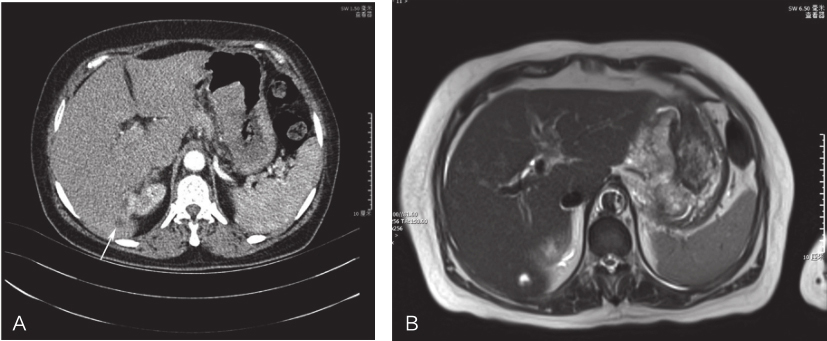
图1腹部影像学提示肝脏转移灶
A.CT图像;B.MRI图像
电子胃镜:胃小弯侧和前后壁可见巨大新生物,表面溃烂,高低不平,苔污秽,取5块组织行活检,质软。余未见异常(图2)。
胃体黏膜活检:(胃体黏膜活检组织)胃肠间质瘤。免疫组织化学染色示:DOG-1(+),CD117(+),CD34(+),S-100(-),PCK(-),CK8/18(-),LCA(-),Syn(-),SDHB(+),Ki-67(Li:30%)。建议手术完整切除肿块后再进一步行病理检查。
初步诊断
1.(胃)胃肠间质瘤伴肝转移
2.轻度贫血
3.2型糖尿病

图2电子胃镜示胃小弯侧和前后壁可见巨大新生物,表面溃烂
【治疗过程】
(一)病例分析
患者为老年女性,因“间断腹痛、腹胀1周余”入院。入院后完善相关检查,腹部CT提示胃癌可能性大(影像学分期T3~4aN1Mx),可能伴有淋巴结转移并不除外肝脏转移;继而进行肝脾MRI检查,结果也提示胃癌伴肝脏转移瘤可能;活检提示胃部原发肿瘤为胃肠间质瘤。目前,患者诊断较为明确:(胃体)胃肠间质瘤伴肝转移。经评估,原发瘤及转移瘤均可完整切除。患者目前一般情况尚可,能耐受手术,故考虑对该患者行手术治疗,一并切除胃部原发瘤及肝脏转移瘤,并根据术后进一步病理检查结果及基因检测结果指导术后药物靶向治疗。
(二)治疗方案
于2017年1月21日剖腹探查,术中发现:胃小弯胃体可见一大小约5cm×6cm的隆起肿物,与周围组织界限清楚,遂行胃部分切除术切除胃部肿瘤;后游离右半肝肝周韧带,充分暴露病灶,发现病灶位于肝右后叶肾上极上方,直径约2cm,质地稍硬。沿病灶外缘1.5cm处用电刀划出预切线,然后离断肝实质,切除肿瘤。术中出血约200ml,两处肿瘤均完整切除,手术过程顺利。
(三)术后病理及基因检测
术后病理:
1.(胃体) GIST伴间质黏液变,胃周淋巴结(1/9)切片上见肿瘤转移,两侧手术切缘上未见肿瘤累及(肿块大小8.5cm×8cm×5cm,核分裂象>10个/50HPF)。
2.(肝脏)转移性胃肠间质瘤伴淋巴组织反应性增生,结合病史、形态学及免疫组织化学染色,符合胃来源,肝手术切缘未见肿瘤累及(图3)。
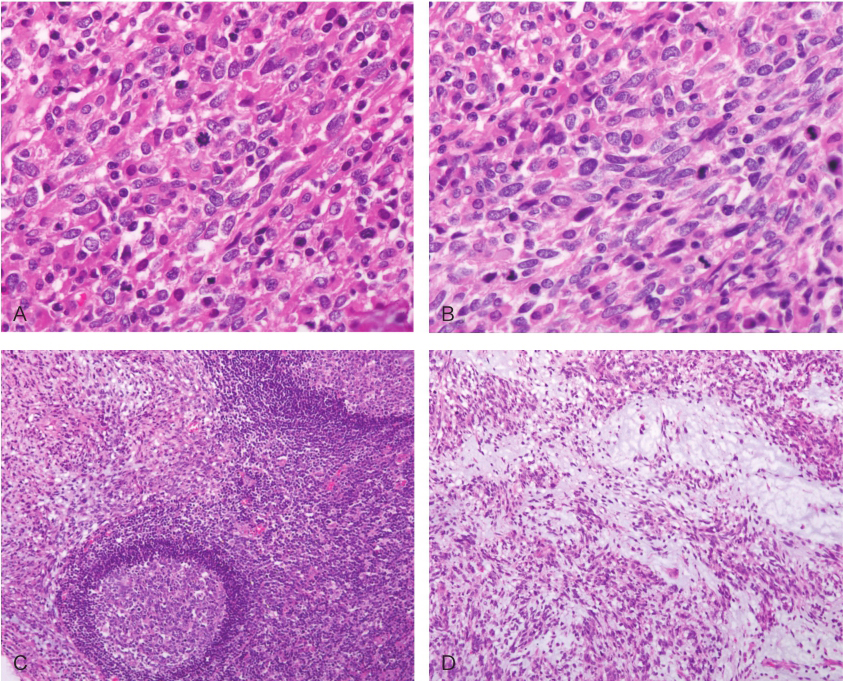
图3术后病理
A.原发灶;B.肝转移;C.淋巴结转移;D.黏液变
免疫组织化学染色示胃原发灶:CD117(+),DOG-1(+),S-100(-),Ki-67(Li:30%),SDHB(+)。
肝脏转移灶:CD117(+),DOG-1(+),SDHB(+),Ki-67(Li:30%)。
基因检测:胃原发病灶及肝转移瘤均为c-KIT基因外显子11发生突变,突变类型为c.1673_1674insTCC;PDGFRA基因外显子12、18为野生型。
【预后】
患者术后恢复顺利,于术后第12天出院。患者术后1个月开始使用伊马替尼辅助治疗,400mg/d,期间出现了眼眶周围严重水肿,双上肢散在皮疹以及腹泻等不良反应,进行利尿、抑酸护胃等相应对症支持治疗后,不良反应仍未缓解。2017年5月监测伊马替尼血药浓度为2423.2ng/ml,遂建议患者减量至300mg/d,不良反应随之减轻,患者可以耐受。两周后监测伊马替尼血药浓度为1548.3ng/ml,患者遂服用伊马替尼300mg/d至今。截至2018年7月,随访18个月,患者未出现肿瘤复发或转移迹象。
【经验与体会】
(一)淋巴结转移是否是GIST疾病发展的晚期事件?
GIST的转移途径主要是血运转移至肝脏或经腹膜直接播散,淋巴结转移则相对少见。针对原发GIST的危险度评估有许多分级分期标准,如NIH危险度分级、AFIP标准以及目前应用最广泛的改良NIH危险度分级等,这些标准均未将淋巴结转移作为评估的参数。而在2009年公布的美国癌症联合委员会(American Joint Committee on Cancer,AJCC)TNM分期系统中,首次将淋巴结转移作为评估GIST生物学行为及预后的因素,并且只要伴有淋巴结转移即归为Ⅳ期,这与传统认识发生了较大的冲突,也存在着很多争议。部分学者认为,淋巴结转移是GIST发病过程中一个较为晚期的事件,发生在血液转移之后,一旦出现,病情往往出现进展或局部侵犯或远处转移。这可能也是AJCC将淋巴结转移归为Ⅳ期的原因之一。也有部分学者认为,不同于消化道上皮源性的肿瘤,淋巴结转移在GIST病程中的地位尚不十分明确,有部分伴有淋巴结转移的患者不出现或较晚才出现肝脏转移,因此淋巴结转移在GIST病程中未必是晚期事件。
国外一项研究分析了美国国立癌症研究所数据库(The Surveillance,Epidemiology,and End Results)中2004年至2014年伴有淋巴结转移的GIST患者预后情况,发现伴有远处转移的患者更有可能出现淋巴结转移。并且,该研究还发现淋巴结转移对于原发GIST患者的总生存期并无影响;而对于伴有远处转移的患者来说,淋巴结转移是一个独立的预后危险因素,同时伴有远处转移和淋巴结转移的患者,其总生存期明显短于仅有淋巴结转移的患者。本例患者确诊时同时发现了肝脏转移及淋巴结转移,术后遵循医嘱规范地行靶向药物治疗,截至2018年7月,该患者未出现肿瘤复发或转移迹象。
(二)应当根据血药浓度来调整伊马替尼剂量
B2222试验的药物动力学研究发现,对于晚期GIST患者,当伊马替尼的血浆谷浓度水平低于1100ng/ml时,伊马替尼的治疗效果会明显降低。因此,保持一定的血浆药物浓度,对于伊马替尼的疗效至关重要。
伊马替尼在大多数患者中有着良好的耐受性。其常见的不良反应包括水肿、胃肠道反应、白细胞减少、贫血、皮疹等;大多数为轻至中度,通过对症治疗即可改善或恢复正常。但是对于部分患者,在标准剂量的伊马替尼治疗中可能出现严重的不良反应。本例患者服用伊马替尼400mg/d期间,出现了一系列局部及全身不良反应,经对症支持治疗后仍未缓解,严重影响了生活质量。NCCN指南指出,对于出现严重不良反应的患者,可以考虑暂时停药或减量至300mg/d。因此,在监测了血药浓度后,我们建议患者先减量至300mg/d。随后,伊马替尼血浆药物浓度降至1548.3ng/ml,不良反应也随之改善。随访至今18个月,并未发现肿瘤复发或转移迹象。
因此,针对患者的个体情况,进行伊马替尼血浆药物浓度监测,制订个性化药物剂量方案,或许是GIST 辅助治疗更为合理的选择。
【专家点评】
胃肠间质瘤作为软组织肉瘤的一种,其淋巴结转移率较低,常规不要求行淋巴结清扫术。但是,对于年轻女性的多结节性胃GIST,SDHB(-),若同时伴有肾上腺肿瘤或肺软骨瘤,考虑为Carney三联征或Carney Stratakis综合征者,由于其淋巴结转移多常见,可考虑行淋巴结清扫术,术前CT或术中发现淋巴结肿大者,也建议行淋巴结清扫术。由于此类患者的生物学行为较好,其预后不能用常见的危险度评估标准,有些患者尽管出现了淋巴结或肝转移等,其预后也较其他类型的GIST更好。但是,在非SDHB缺陷型GIST中,淋巴结转移是预后的独立危险因素。此患者为c-KIT 外显子 11突变的GIST患者,因而不属于SDHB缺陷型GIST患者,且不仅有淋巴结转移,同时也出现了肝转移,应积极地进行靶向治疗。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。 此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
[1]中国临床肿瘤学会胃肠间质瘤专家委员会. 中国胃肠间质瘤诊断治疗共识 (2017年版) [J] . 肿瘤综合治疗电子杂志, 2018, 4 (1) : 31-43.
[2]DEMATTEO R P, LEWIS J J, LEUNG D, et al. Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival [J] . Ann Surg, 2000, 231 (1) : 51-58.
[3]汪明, 曹晖, 金鑫, 等. 胃肠道间质瘤淋巴结转移的临床及病理特征分析 [J] . 外科理论与实践杂志, 2011, 3 (16) : 298-300.
[4]VON MEHREN M, RANDALL R L, BENJAMIN R S, et al. Soft Tissue Sarcoma, Version 2. 2018, NCCN Clinical Practice Guidelines in Oncology [J] . J Natl Compr Canc Netw, 2018, 16 (5) : 536-563.
[5]孔梅, 王艳丽, 许林杰, 等. 小肠的恶性胃肠道间质瘤伴淋巴结转移病理分析 [J] . 中华病理学杂志, 2009, 9 (38) : 617-620.
[6]陶凯雄, 张鹏. 胃肠间质瘤精准诊疗与全程化管理 [M] . 武汉: 湖北科学技术出版社, 2018, 8: 40-41.
[7]GAITANIDIS A, EL LAKIS M, ALEVIZAKOS M, et al. Predictors of lymph node metastasis in patients with gastrointestinal stromal tumors (GIST) [J] . Langenbecks Arch Surg, 2018, 403 (5) : 599-606.
[8]王超, 高志冬, 申占龙, 等. 腹腔镜手术与开腹手术行食管胃结合部胃肠间质瘤切除的疗效比较 [J] . 中华胃肠外科杂志, 2015, (9) : 881-884.
人卫知识数字服务体系





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
