结直肠为胃肠间质瘤(gastrointestinal stromal tumor,GIST)相对少发部位,仅占全部GIST的4%~6%,其中原发于结肠的GIST更为罕见。结肠GIST多发生于成年人,尤以女性多见。最好发于乙状结肠,其次为横结肠。临床症状与发生的部位、肿瘤大小有关,可表现为大便习惯改变、便血或腹痛、肠梗阻等,亦可无明显临床症状,仅在体检时发现。因其发生率低,文献中缺少针对结肠GIST的描述与报道,易被临床忽视。
【病例摘要】
患者,男性,52岁,因“反复左下腹痛1年”就诊。患者1年前无明显诱因出现左下腹疼痛,呈阵发性绞痛,排便前尤甚,排便后可缓解,疼痛无向他处放射,与体位无明显关系。无其他不适,未行特殊治疗。1周前在当地医院查肠镜示:横结肠息肉,乙状结肠黏膜下隆起性病变。起病以来,患者饮食正常,体重无明显减轻。
既往史及家族史
胆囊结石病史8年,未行特殊治疗。否认食物及药物过敏史。父母健在,家族中无类似病史。
体格检查
生命体征平稳。腹部平坦,未见胃肠型及蠕动波。腹肌软,全腹无明显压痛、反跳痛,未触及肿物,墨菲征阴性,移动性浊音阴性,肠鸣音正常。
辅助检查
血常规、血生化、凝血功能及肿瘤标志物:未见明显异常。
全腹彩超:下腹腔低回声包块,性质待定,建议进一步检查;脂肪肝;胆囊多发结石;胆囊多发息肉;双肾多发囊肿。
全腹增强MRI:左下腹见一类圆形异常信号影,考虑结肠间质来源肿瘤;脂肪肝;胆囊多发结石;双肾多发囊肿(图1)。
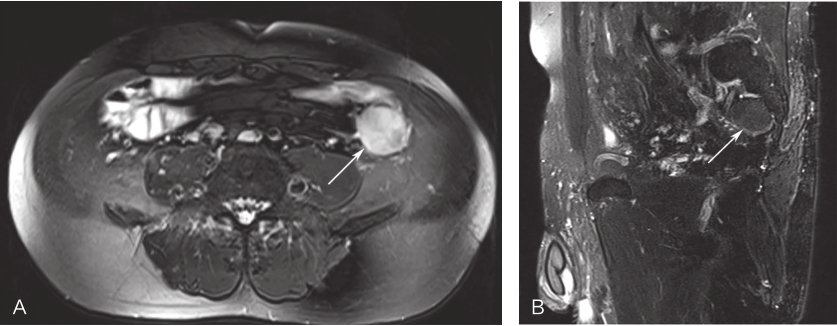
图1 腹部MRI
A.横断面;B.矢状面,左下腹见一类圆形异常信号影,结肠GIST
超声肠镜:乙状结肠黏膜下隆起性低回声肿物,3.9cm×3.3cm,边界尚清,起源于第四层,可见部分彩色血流,GIST可能?
初步诊断
1.乙状结肠黏膜下肿瘤:GIST可能
2.胆囊多发结石
3.胆囊多发息肉
4.脂肪肝
5.双肾多发囊肿
【治疗过程】
(一)病例分析
患者为中年男性,一般状况良好。影像学检查提示乙状结肠肿物,GIST可能。经评估可完整切除,建议手术切除肿物,明确诊断再行下一步诊治。
(二)治疗方案
于2017年11月14日行“腹腔镜下乙状结肠部分切除术”,术中所见:腹腔内无腹水,肝脏、盆腔未见转移瘤。乙状结肠上段肿瘤约4.0cm×4.0cm,位于黏膜下,突向肠腔,界限清楚,与周围组织无粘连。肠旁、乙状结肠动脉旁、肠系膜下血管根部未见明显肿大淋巴结。手术过程顺利。
(三)术后病理及基因检测
术后病理:(乙状结肠)胃肠间质瘤,大小4.0cm×3.8cm×3.5cm,梭形细胞型,核分裂象:5个/50HPF;改良NIH危险度分级:低危。肠旁淋巴结未见转移(0/8),呈反应性增生(图2)。
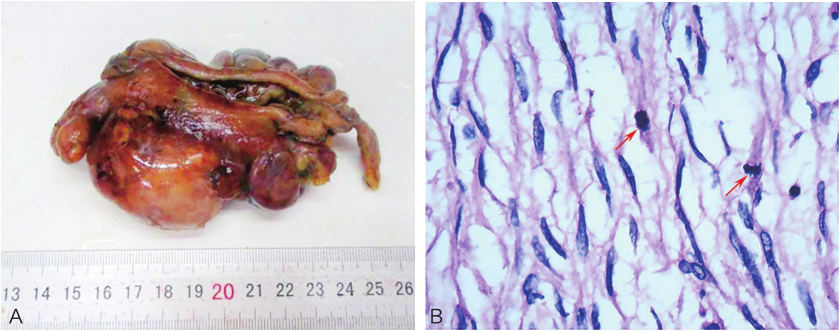
图2 术后病理
A.肿瘤大体标本;B.HE染色×40倍,可见核分裂象
免疫组织化学染色:乙状结肠肿瘤:CD117(+),CD34(+),DOG-1(+),SMA(-),desmin(-),Ki-67(Li:约 2%)。
基因检测:c-KIT基因外显子9突变。
【预后】
患者术后30小时肛门排气,72小时进食半流质饮食,术后6天顺利出院。术后第11天给予伊马替尼治疗,400mg/d。术后1年复查未见肿瘤复发转移,无明显不良反应。
【经验与体会】
手术是局限性原发结直肠GIST的主要治疗方法。与恶性肿瘤外科手术原则一样,结直肠GIST同样须遵守“无瘤、无菌”手术原则。进行肿瘤的完整切除是结直肠GIST长期生存的最重要保证。但不同于结直肠癌,GIST很少通过淋巴管转移,跳跃性转移更为罕见。因此不需要进行广泛切除或全直肠系膜切除,建议采用节段性结直肠切除术保证切缘阴性即可。以降期及缩小肿瘤为目的的术前治疗可以降低术中医源性肿瘤播散的风险,保存重要脏器功能,对于较大的肿瘤或位于直肠下段的GIST,术前靶向治疗有重大意义。
【专家点评】
结直肠为GIST相对少发部位,原发于结肠的GIST更为罕见。结肠GIST多发生在成年人,尤以女性多见。最好发于乙状结肠,其次为横结肠,再次为降结肠,升结肠及盲肠发病率最低。目前结合直肠指诊、内镜、EUS、MRI、CT等检查手段,诊断结直肠GIST并不困难。手术是局限性原发结直肠GIST的主要治疗方法,肠段切除即可,无需清扫淋巴结。对于较大的肿瘤或位于直肠下段的GIST,术前靶向治疗有重大意义,既可增加R0切除的概率,又可最大限度地保留功能。术后应完善病理学检查和基因检测,指导辅助治疗的实施。术后诊断为中高危的结直肠GIST应服用伊马替尼治疗。2017版CSCO专家共识推荐中危结直肠GIST术后伊马替尼辅助治疗3年,高复发风险者辅助治疗时间至少为3年;发生肿瘤破裂者,可以考虑延长辅助治疗时间。至于低危患者是否需要服药,目前没有证据支持,但是对于中低危交界患者,可以考虑术后服用伊马替尼治疗。
免责声明
内容来源于人卫知识数字服务体系、人卫inside知识库,其观点不反映优医迈或默沙东观点。 此服务由优医迈与胤迈医药科技(上海)有限公司授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
[1] MIETTINEN M, LASOTA J. Gastrointestinal stromal tumors: pathology and prognosis at different sites [J] . Semin Diagn Pathol, 2006, 23 (2) : 70-83.
[2]SCMIDE K, SANDVIK O M, SCREIDE J A, et al. Global epidemiology of gastrointestinal stromal tumours (GIST) : A systematic review of population-based cohort studies [J] . Cancer Epidemiol,2016, 40: 39-46.
[3]FENG F, TIAN Y, LIU Z, et al. clinicopathological features and prognosis of colonic gastrointestinal stromal tumors: evaluation of a pooled case series [J] . Oncotarget, 2016, 7 (26) : 40735-40745.
[4] JOENSUU H, VEHTARI A, RIIHIMÄKI J, et al. Risk of recurrence of gastrointestinal stromal tumour after surgery: an analysis of pooled population-based cohorts [J] . Lancet Oncol, 2012, 13 (3) : 265-274.
[5]陶珊, 张鹏. 结直肠胃肠间质瘤临床病理特点与治疗策略探讨 [J] . 临床消化病杂志, 2018, 30 (3) : 194-197.
[6]DEMATTEO R P, GOLD J S, SARAN L, et al. Tumor mitotic rate, size, and location independently predict recurrence after resection of primary gastrointestinal stromal tumor (GIST) [J] . Cancer, 2008, 112 (3) : 608-615.





 Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2025 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
