21岁女学生,入院前半个月无明显诱因出现咳嗽、咳痰,并发热,未重视。10天前症状加重,伴有呼吸困难,至当地医院,对症处理后无改善,并出现氧合进行性下降,行经口气管插管接呼吸机辅助通气,气道内可吸出大量血性痰液,予积极抗感染(应用抗生素:伏立康唑、利奈唑胺、比阿培南以及奥司他韦)、激素冲击、提高免疫力以及加强气道管理等治疗,病情仍未改善,患者持续高热,最高体温达40℃。为进一步治疗,转入笔者医院ICU。
【病情介绍】
患者,女性,21岁,学生。因“咳嗽伴发热半个月,加重10天”于2011年1月4日入院。患者入院前半个月无明显诱因出现咳嗽、咳痰,并发热,未重视。10天前症状加重,伴有呼吸困难,至当地医院,对症处理后无改善,并出现氧合进行性下降,行经口气管插管接呼吸机辅助通气,气道内可吸出大量血性痰液,予积极抗感染(应用抗生素:伏立康唑、利奈唑胺、比阿培南以及奥司他韦)、激素冲击、提高免疫力以及加强气道管理等治疗,病情仍未改善,患者持续高热,最高体温达40℃,气道内仍可吸出大量血性痰液(痰培养提示鲍氏不动杆菌,MDR),呼吸机支持条件加至PEEP 12~15cmH2O、FiO2 60%~70%,经皮血氧饱和度仅可维持在85%左右,伴有循环波动,多巴胺6μg/(kg•min)持续静脉泵入,血压可维持在90/50mmHg左右,心率150次/分,为进一步治疗,由外院转入笔者医院ICU。既往健康,否认肺结核、肝炎等病史,否认外伤史,否认家禽接触史。
体格检查:T 36.8℃,P 150次/分,R 22次/分,BP 75/42mmHg[多巴胺6μg/(kg•min)持续静脉泵入]。镇静,Ramsay评分4分,气管插管接呼吸机治疗(SIMV和PS模式:Vt 380ml、FiO2 60%、PEEP 15cmH2O、PS 10cmH2O、F 20次/分),双肺呼吸音对称,呼吸音粗,散在大量干湿性啰音,心率150次/分,律齐,心电监护提示频发室性期前收缩及室上性心动过速,二尖瓣区可闻及收缩期隆隆样杂音(2/6级),余未查见阳性体征。
辅助检查:动脉血气分析:pH 7.52,PaCO2 37mmHg,PaO2 77mmHg,PaO2/ FiO2 137mmHg,Lac 3.6mmol/L, 27.3mmol/L;血常规:WBC 33.01×109/L,Hb 81g/L,PLT 100×109/L,N 92.1%;外周血培养(外院)示溶血性葡萄球菌(对利奈唑胺、万古霉素敏感)。TnI 0.1ng/ml。BNP 524pg/ml。
入院诊断:①病毒性肺炎,细菌性肺炎,急性呼吸衰竭(Ⅰ型),急性呼吸窘迫综合征;②血源性感染;③感染性休克;④中毒性心肌炎;⑤急性感染性心内膜炎;⑥心律失常:室性期前收缩,短暂性阵发性室性心动过速。
诊疗经过:入院后治疗分为3个阶段:
第一阶段(入院后第1~6天):考虑重症感染、感染性休克,考虑感染来源肺部感染以及血源性感染,故予利奈唑胺、头孢哌酮-舒巴坦钠、左氧氟沙星抗感染治疗,并加强气道管理,俯卧位通气,患者氧合改善不明显,故床边行体外膜肺氧合治疗(VV-ECMO模式),氧合明显好转,但循环仍有波动,外院血培养回报溶血性葡萄球菌,加用达托霉素治疗,但入院后第5天,患者心脏功能恶化,血压不能维持,乳酸进行性升高,最高13.0mmol/L,不能耐受液体,床边心脏超声检查提示重度二尖瓣关闭不全,二尖瓣赘生物。床边将ECMO模式改为VV-ECMO与VA-ECMO并行,辅助循环及呼吸功能,维持循环及氧合,保证组织灌注,并急诊在全麻低温体外循环下行二尖瓣置换术。
第二阶段(入院后第7~26天):二尖瓣置换术后患者心功能明显改善,多次复查心脏超声均提示心脏舒张及收缩功能未见明显异常,瓣膜功能良好。但患者感染难以控制,考虑感染源:①肺部感染:无法脱离ECMO,胸片提示双肺渗出影(图1),多次痰培养结果均提示鲍曼不动杆菌(MDR);②血源性感染:多次外周血及导管血培养提示洋葱伯克霍尔德菌;③感染性心内膜炎:考虑患者存在急性感染性心内膜炎,瓣膜赘生物形成,多为革兰阳性杆菌感染,但赘生物培养却未见细菌生长。鉴于以上感染相关证据,调整抗感染治疗方案为达托霉素和美罗培南联合左氧氟沙星,并加强气道管理,入院24天后病情明显好转,感染得到控制,逐渐增加呼吸机支持条件,并降低ECMO辅助条件,患者氧合及循环情况均未见恶化,复查胸片渗出较前吸收(图2~图4),故入院后第26天脱离ECMO,在常规机械通气的情况下,患者指脉氧饱和度可维持在95%左右,监测乳酸在1.0mmol/L左右,经皮氧分压88mmHg,经皮二氧化碳分压50mmHg。
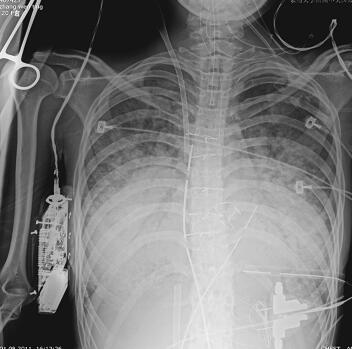
图1 开始ECMO胸片
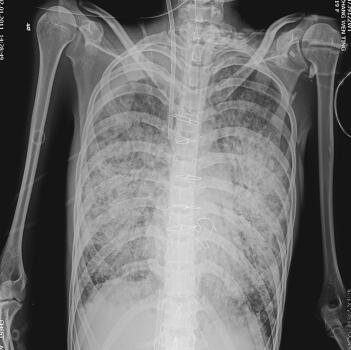
图2 入院第26天胸片
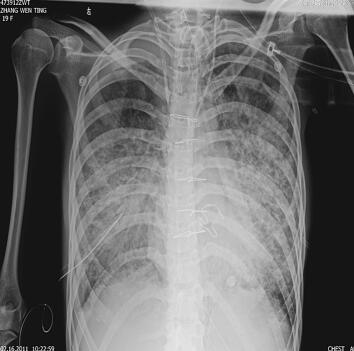
图3 ECMO撤离前
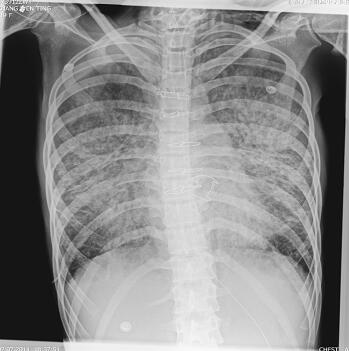
图4 ECMO撤离后
第三阶段(入院后第27~46天):患者病情好转,常规机械通气,SIMV和PS模式:Vt 380ml、PEEP 8cmH2O、PS 15cmH2O、FiO2 50%,监测指脉氧饱和度在93%~97%之间,血压在去甲肾上腺素2μg/min持续静脉泵入可维持在110/60mmHg,但出现并发症:①气胸:反复出现气胸(图5A、B),前后共行胸腔闭式引流术8次,随着肺部感染进一步好转,气胸痊愈(图5C、D);②急性肾衰竭:感染性休克导致肾灌注不足,出现急性肾衰竭,持续无尿状态,床边CRRT治疗;③气道出血:患者出现气道出血,予积极止血、气道管理等处理,病情一度好转,但发病后46天患者再次出现气道出血,氧合难以维持,最终死亡。
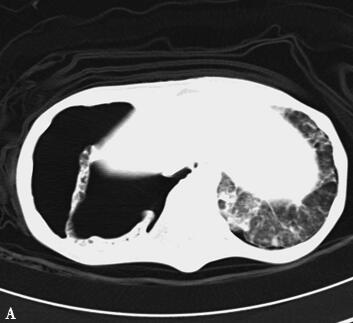
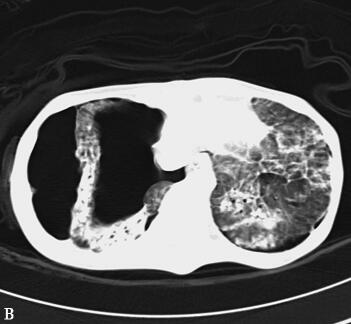
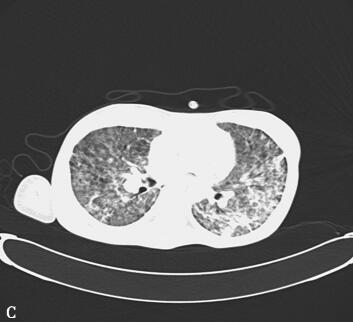
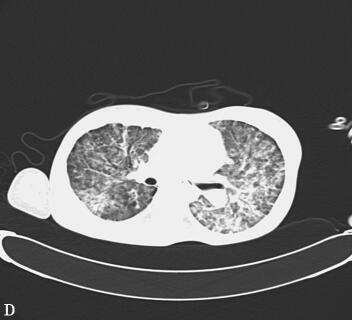
图5胸部CT(A、B.气胸C、D.气胸痊愈)
重要提示
1.年轻女性,突发发热,伴呼吸困难入院。
2.急性感染性心内膜炎,急性起病,心前区可闻及杂音,床边心脏超声提示二尖瓣重度关闭不全,二尖瓣赘生物形成;手术证实。
3.严重ARDS较高机械通气条件下氧合仍难以维持,氧合指数仅可维持在100mmHg左右。
4.严重感染、感染性休克 感染较难控制,循环难以维持,需血管活性药物干预。
5.并发症,严重感染并发肺纤维化,多次出现气胸,需反复多次穿刺留置胸腔闭式引流;气道出血;肾衰竭。
【讨论】
1.感染性心内膜炎的治疗——千钧一发
感染性心内膜炎为心脏内膜表面的微生物感染,伴赘生物形成,瓣膜为最常受累部位,但感染也可发生在间隔缺损部位、腱索或心壁内膜。根据病程分为急性和亚急性,急性感染性心内膜炎特征:①中毒症状明显;②病程进展迅速,数天至数周引起瓣膜破坏;③感染迁移多见;④病原体主要为金黄色葡萄球菌。急性感染性心内膜炎通常病原体是在身体某部位发生感染,当机体抵抗力降低时,细菌入血侵犯心内膜,主要侵犯二尖瓣和主动脉瓣,引起急性化脓性心瓣膜炎,在受累的心瓣膜上形成赘生物。受累瓣膜可发生破裂、穿孔或腱索断裂,引起急性心瓣膜功能不全。治疗上需给予积极抗感染治疗,疗程较长,而对于有些严重心内并发症或抗生素治疗无效者则考虑手术治疗。
本例患者在出现上呼吸道感染症状后继发呼吸困难,且出现血性痰液,查体发现二尖瓣听诊区存在杂音,心脏超声检查明确诊断,患者出现心源性休克、循环难以维持。虽然赘生物培养未见细菌生长,但考虑可能与病程前期反复应用多种抗生素有关,同时不能排除假阴性结果,根据流行病学调查结果考虑感染性心内膜炎,病原体多为革兰阳性菌,患者存在肾功能不全,限制了万古霉素的使用,考虑到达托霉素在皮肤软组织及瓣膜有较高的组织浓度,故加用达托霉素抗感染治疗。经手术治疗去除感染性赘生物、换瓣后,心功能明显改善,ECMO的支持模式由同时辅助循环呼吸功能的VA模式改为VV模式辅助呼吸功能。因此,对于感染性心内膜炎的患者,出现腱索断裂、重度二尖瓣关闭不全而明显影响血流动力学时应积极手术,ECMO有利于维持心源性休克患者围术期的循环稳定,保证器官灌注。
2.多药耐药菌的防治——艰难困苦
随着抗菌药物的广泛应用,各种耐药菌不断出现,如耐青霉素肺炎链球菌(Penicillin-resistant streptococcus pneumoniae,PRSP)、耐甲氧西林金黄色葡萄球菌(Methicillin-resistant staphylococcus aureus,MRSA)、耐万古霉素肠球菌(Vancomycin-resistant Enterococcus,VRE)、耐药革兰阴性杆菌和多重耐药结核分枝杆菌等,其中有些耐药菌感染目前尚无有效的治疗药物。目前多药耐药菌不断出现,已经成为全世界公认的难题。多药耐药(multi-drug resistance,MDR)是指细菌同时对三类或三类以上抗菌药物耐药,如头孢菌素类、喹诺酮类、氨基糖苷类抗生素;其产生的主要原因在于滥用抗生素,因此,需要重新认识抗生素,并且关注MDR细菌的治疗。ICU患者由于病情危重、免疫功能低下、住院时间长、大量使用抗菌药物及接受多种侵入性检查和治疗,细菌耐药性不断增强,普遍呈现高度耐药、多药耐药态势。
本例患者治疗过程,虽然在不同治疗阶段治疗策略和重点不同,但是均围绕一个难题:感染控制。回顾整体诊疗过程,患者出现多药耐药菌感染存在一定诱因。首先,患者外院治疗期间曾应用多种抗生素,如利奈唑胺、伏立康唑、亚胺培南等,容易诱导细菌耐药;其次,患者发病后持续应用糖皮质激素治疗,加之本身疾病的影响,患者淋巴细胞免疫功能始终处于中度免疫功能抑制状态。此患者入笔者医院后主要感染源为肺部感染及血源性感染,积极做好单位隔离、手卫生、气道管理、管道护理等非抗生素抗感染治疗措施,并采取联合抗生素治疗方案,使感染得到控制,患者能脱离ECMO,常规机械通气即可维持氧合,且器官功能好转。
3.严重急性呼吸窘迫综合征的治疗——六步法
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是发生于严重感染、休克、创伤及烧伤等疾病过程中,由于肺毛细血管内皮细胞和肺泡上皮细胞损伤引起弥漫性肺间质及肺泡水肿,并导致以进行性低氧血症、呼吸窘迫为特征的临床综合征。X线胸片呈现斑片状阴影为其影像学特征;肺容积减少、肺顺应性降低和严重的通气与血流比例失调为其病理生理特征。临床上表现为进行性低氧血症和呼吸窘迫,肺部影像学上表现为非均一性渗出性病变。对于严重ARDS尚缺乏统一的诊断标准,满足以下四条中的一条即可:①肺损伤评分> 3分;②难治性低氧血症(FiO2>80%时,PaO2<90mmHg,持续1小时以上);③顽固性酸中毒(pH>7.10,持续1小时以上);④气道平台压持续高于35~40cmH2O(Vt 4~6ml/kg)。现有的治疗手段主要包括病因治疗(感染、创伤、休克等原发病治疗以及液体管理)、呼吸支持(小潮气量肺保护性通气、肺开放、维持肺开放、俯卧位、高频振动通气和体外膜氧合技术等)以及药物治疗(糖皮质激素、吸入NO和补充表面活性蛋白等),即便如此,ALI/ARDS的病死率仍高达30%~40%,因此,顽固性ARDS的机械通气治疗面临着挑战,在现有治疗方法的基础上,目前提出ARDS治疗的六步法:
步骤1:测量气道平台压力,如果<30cmH2O,进入步骤2a;如果>30cmH2O,进入步骤2b。
步骤2a:实施肺复张和(或)使用高PEEP。
步骤2b:实施俯卧位通气或高频振荡通气。
步骤3:评价氧合改善效果、静态顺应性和无效腔通气,如果改善明显则继续治疗;如果改善不明显,则进入下一步。
步骤4:吸入NO治疗,如果几小时内没有反应,则进入下一步。
步骤5:给予糖皮质激素治疗,个体化评价患者的风险与收益。
步骤6:考虑实施体外生命支持,入选者高压通气时间须小于7天。
每一步骤实施后,都应仔细评价氧合改善效果、静态顺应性和无效腔通气。如果改善明显则继续治疗。如果改善不明显,则进入下一步。
本例属于严重ARDS,治疗上同样适用ARDS六步法,但在实施过程中相关干预措施的选择存在一定限制。首先,患者入院时监测气道平台压较高,已经超过30cmH2O,因此肺复张以及高PEEP的手段不适用,而对于高频机械通气,考虑患者血流动力学不稳定,属于相对禁忌,故立即采取俯卧位通气;其次,患者俯卧位通气数小时,监测指脉氧饱和度无明显改善,且气道平台压下降亦不明显,二氧化碳分压呈现上升的趋势,因此可进入以下步骤,NO的治疗尚存争议,暂时不采用,而糖皮质激素治疗自发病开始即已经开始,氧合等多指标均未见明显改善,且有加重的趋势,故无增加剂量的指征;最后,选择ECMO进行支持,而ECMO的模式选择时则需评估心功能以及肺功能的状况,早期由于患者心脏器质性病变,心功能恶化,需要VA-ECMO辅助呼吸功能的同时兼顾心功能,而在心脏换瓣术后心功能明显改善,即可仅对呼吸功能进行辅助,因此改为VV-ECMO维持患者氧合。可以说,此患者ARDS的治疗经历了评估中选择、选择中评估的历程。
ARDS治疗的六步法能在很大程度上治疗低氧血症,纠正严重酸中毒,有利于临床工作的开展,但各项干预措施均存在一定适用人群,所有治疗措施仍需要以临床医师对患者病情作出正确判断为前提,因此,临床医师的经验在治疗中所起的作用亦不容忽视。
【专家析评】
临床上,重症肺炎、ARDS合并急性细菌性心内膜炎并不常见。早期的心脏查体十分关键,若忽视了心音的听诊等基本检查,很有可能漏诊,丧失最佳治疗时机。当出现腱索断裂、瓣膜关闭不全等急性并发症,循环明显受影响时,果断手术是明智的选择。
多药耐药菌的抗生素选择及治疗疗程是目前抗感染治疗的难题。除了合理使用抗生素外,还应采取以下干预措施:①强化医务人员的医院感染意识,切实落实手卫生规范制度。②加强多药耐药菌的专项监测,并将监测的结果及时反馈至临床,及时有效地采取隔离措施。出现多药耐药菌时,落实消毒隔离措施,明示隔离标志;医护人员在接触患者时应遵循标准预防措施,戴手套和穿隔离衣,治疗护理后及时彻底洗手或用快速手消毒剂消毒;撤销隔离后;床单位终末消毒。③建立、健全合理使用抗菌药物的制度和评价质控体系,优化抗菌药物应用策略,临床医师使用抗菌药物之前应采集病原学标本,根据病原学药敏结果结合临床选用抗菌药物,同时亦需根据药代学和药效学相结合的原则给药。
参考文献
1.叶任高,陆再英.内科学.第6版.北京:人民卫生出版社,325-331.
2.Kollef MH. The intensive care unit as a research laboratory developing strategies to prevent antimicrobial resistance. Surg Infect,2006,7(2):85-99.
3.富秀玉,马桂霞.医院多药耐药菌目标监测的调查与干预措施.中华医院感染学杂志,2011,21:1615-1616.
4.Podnos YD,Cinat ME,Wilson SE,et al. Eradication of multi-drug resistant Acinetobacter from an intensive care unit. Surg Infect,2001,2:297-301.
5.Diaz JV,Brower R,Calfee CS,et al. Therapeutic strategies for severe acute lung injury. Crit Care Med,2010,38:1644-1650.
6.Rubenfeld GD,Herridge MS. Epidemiology and Outcomes of Acute Lung Injury. CHEST,2007,131:554-562.
(环球医学编辑:余霞霞)
免责声明
版权所有©人民卫生出版社有限公司。 本内容由人民卫生出版社审定并提供,其观点并不反映优医迈或默沙东观点,此服务由优医迈与环球医学资讯授权共同提供。
如需转载,请前往用户反馈页面提交说明:https://www.uemeds.cn/personal/feedback
来源:《急诊临床病案评析:感染与心血管性疾病》
作者:陈旭岩 王仲
页码:352-358
出版:人民卫生出版社





 Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.
Copyright © 2023 Merck & Co., Inc., Rahway, NJ, USA and its affiliates. All rights reserved.